
君も化学者! ドライアイスに光を灯そう!
実験は必ず理科の先生と一緒に行ってください。実験するときは,保護めがねを着用してください。
この実験は,ベニヤ板を実験台に敷き,その上で行ってください。
準備するもの
- ドライアイス 2枚(25〜30 cm四方,厚さ7 cm程度のもの)
- マグネシウム粉末
- マグネシウムリボン5 cm程度
- はんだごて
- ハンドバーナー
- 薬さじ
- ベニヤ板
- 冷凍庫用革手袋
- 実験用保護板(透明なプラスチック製のもの)
実験方法1
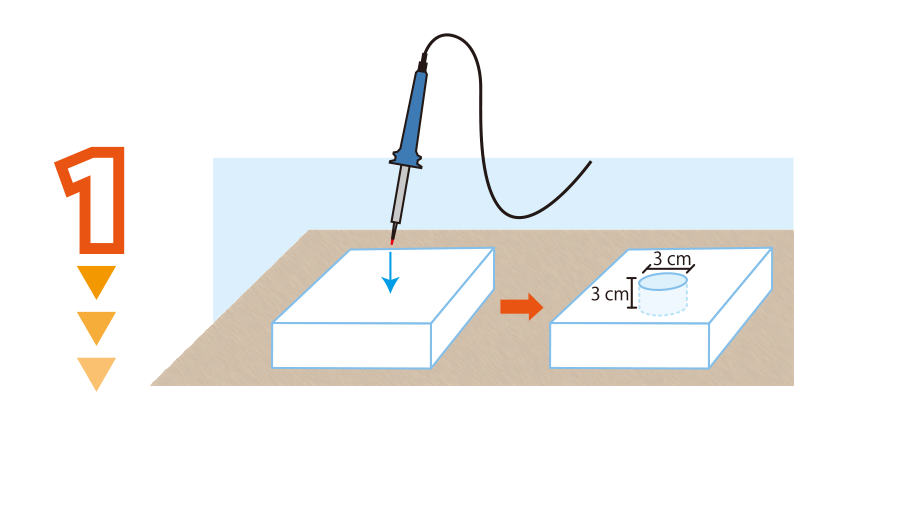
ドライアイス2枚のうち,1枚の中心部分に,はんだごてを用いて直径3 cm,深さ3 cm程度のくぼみをつくる
実験方法2
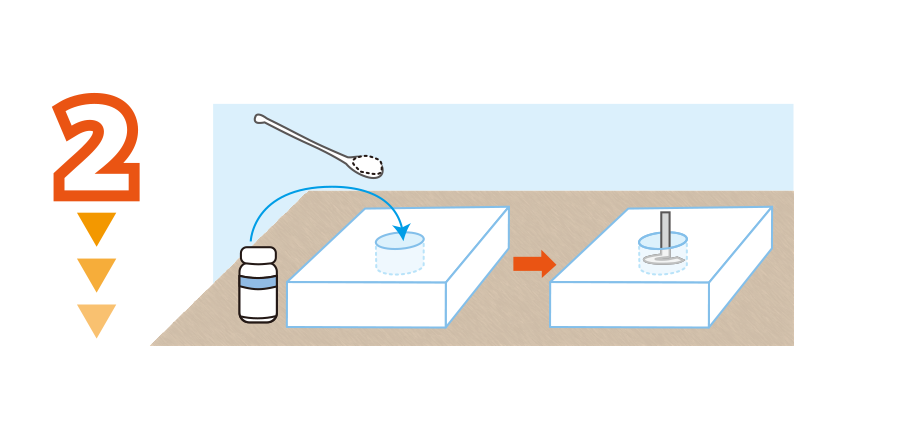
くぼみに,薬さじ一杯程度のマグネシウム粉末を入れ,その中心に 5 cm程度のマグネシウムリボンを立てる
実験方法3
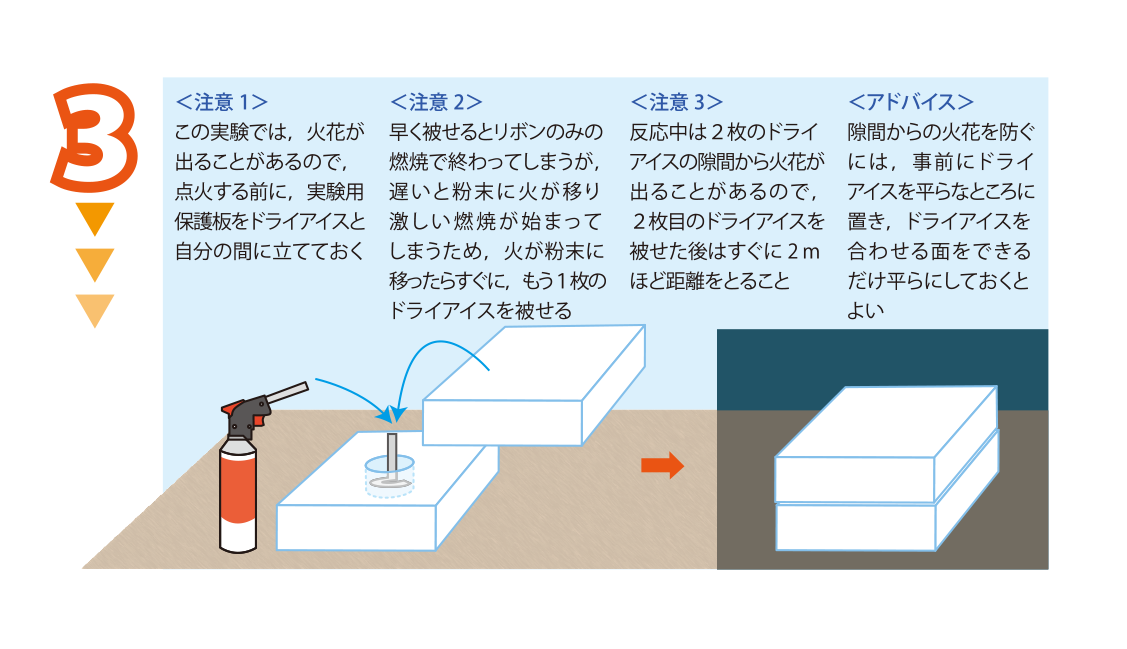
ハンドバーナーを使ってマグネシウムリボンの先端に点火する
火がリボンから粉末に移ったらすぐに,もう1枚のドライアイスを被せ,部屋を暗くする
<注意1>この実験では,火花が出ることがあるので,点火する前に,実験用保護板をドライアイスと自分の間に立てておく
<注意2>早く被せるとリボンのみの燃焼で終わってしまうが,遅いと粉末に火が移り激しい燃焼が始まってしまうため,火が粉末に移ったらすぐに,もう1枚のドライアイスを被せる
<注意3>反応中は2枚のドライアイスの隙間から火花が出ることがあるので,2枚目のドライアイスを被せた後はすぐに2 mほど距離をとること
<アドバイス>隙間からの火花を防ぐには,事前にドライアイスを平らなところに置き,ドライアイスを合わせる面をできるだけ平らにしておくとよい
実験方法4
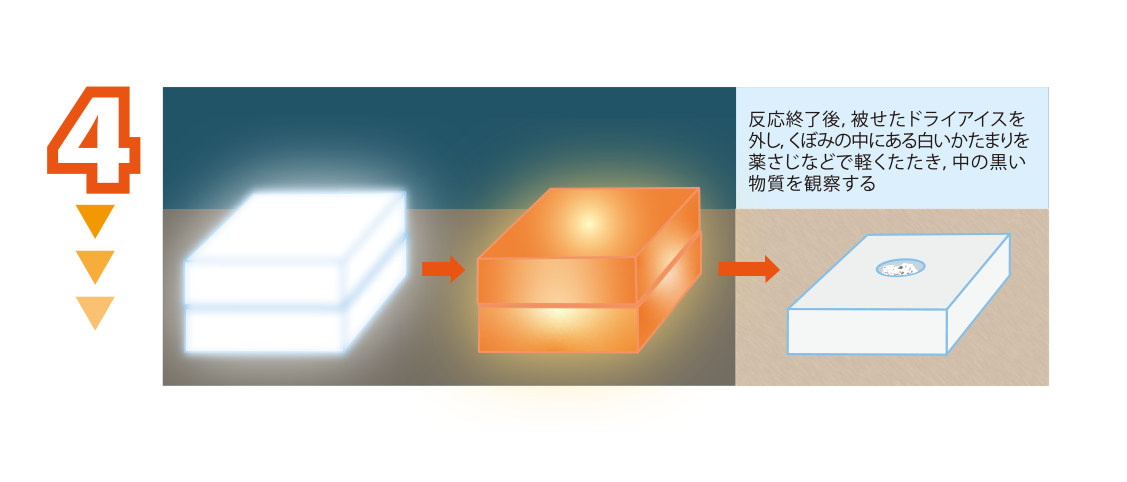
ドライアイス全体が,白く光った後,赤みを帯びた光に変化して反応が終了する
反応終了後,被せたドライアイスを外し,くぼみの中にある白いかたまりを薬さじなどで軽くたたき,中の黒い物質を観察する
実験の解説
マグネシウムMgは燃焼しやすいため,二酸化炭素CO2中でも二酸化炭素から酸素を奪って,光と熱を発しながら燃焼します。そのため,空気を断っても二酸化炭素の個体であるドライアイスの中で燃焼し続けることができます。
2Mg + CO2 → 2MgO + C
反応後には,白い物質である酸化マグネシウムMgOと,黒い物質の炭素Cが残ります。実験方法4でドライアイス全体が白く光るのは,マグネシウムが燃焼すると激しい白い光を放つからです。また,途中でドライアイス全体が赤っぽくなるのは,反応によって生じた炭素が熱せられたからです。
化学だいすきクラブニュースレター第52号(2022年12月1日発行)より編集/転載




