
君も化学者! キラキラ光る自然発火
実験は必ず理科の先生と一緒に行ってください。
実験するときは,保護めがね着用してください。
準備するもの
- シュウ酸鉄(II)二水和物
- 薬包紙
- 薬さじ
- 電子天秤
- 試験管
- コルク栓
- 金属製の試験管ばさみ
- ガスバーナー
- ガスライター
- ろ紙
- 金属製の試験管立て
- 新聞紙
- 霧吹き
- 砂場(金属製のトレイに砂を敷き詰めたもの)
実験方法1
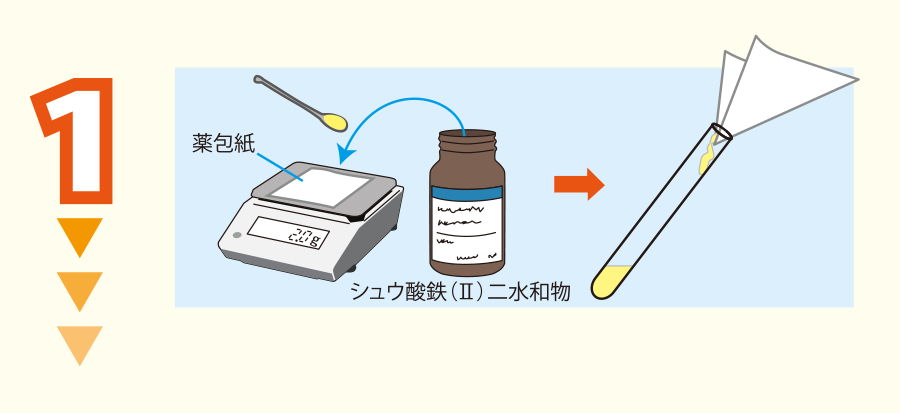
シュウ酸鉄(II)二水和物を約2 gはかり取り,試験管に入れる。
実験方法2
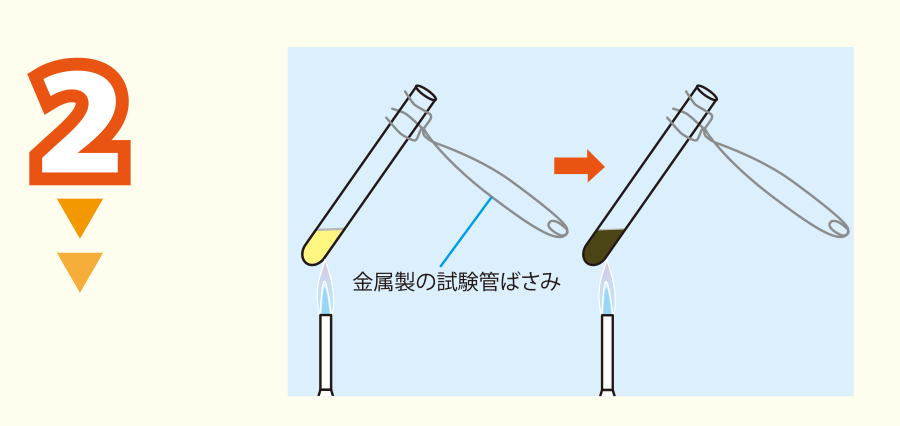
試験管を金属製の試験管ばさみではさみ,シュウ酸鉄(Ⅱ)二水和物が黄色から黒色になるまで加熱する
<アドバイス1>試験管の内壁に水がつくので,時々試験管全体を加熱し水を蒸発させる。
<アドバイス2>時々,試験管を振り,シュウ酸鉄(Ⅱ)二水和物が完全に黒くなるまで加熱する。
実験方法3
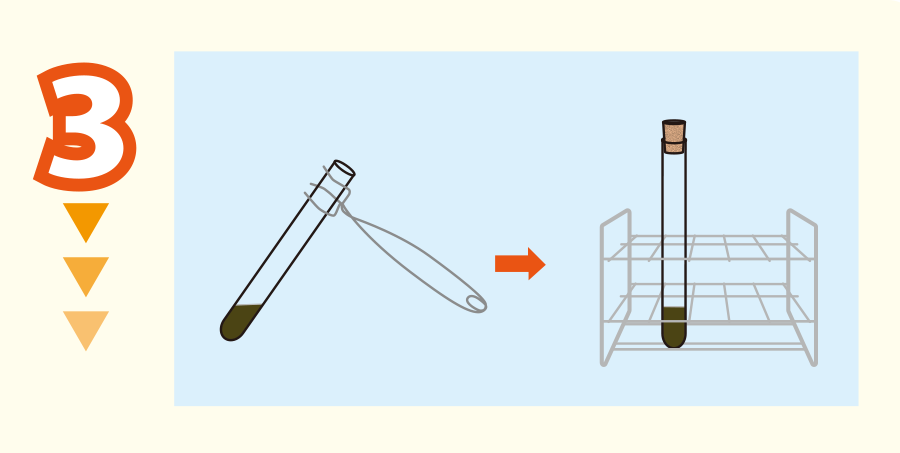
完全に黒色になったら加熱を止める。試験管に軽くコルク栓をし,しばらく放置して冷ます。
<アドバイス>試験管の口あたりに水滴が残っていたら,ろ紙辺で水分を拭き取る
実験方法4
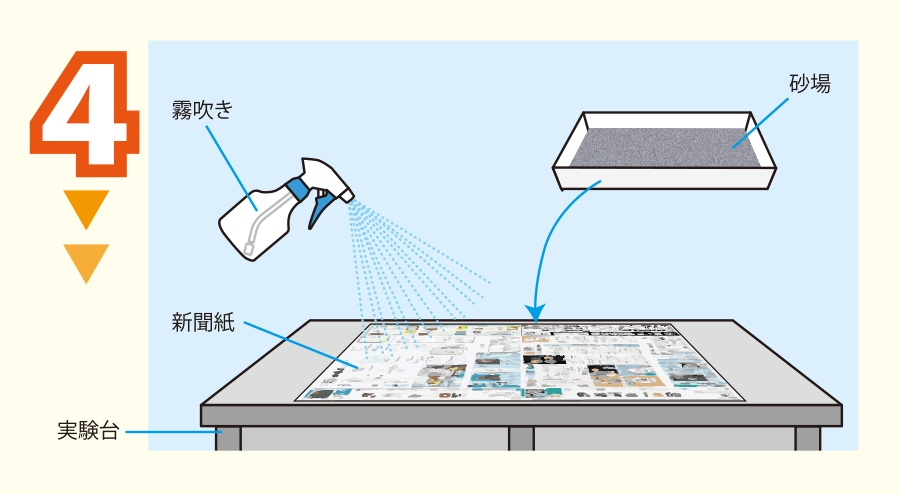
実験台に新聞紙を敷き,霧吹きの水で濡らす。
その新聞紙の上に砂場を置く。
実験方法5
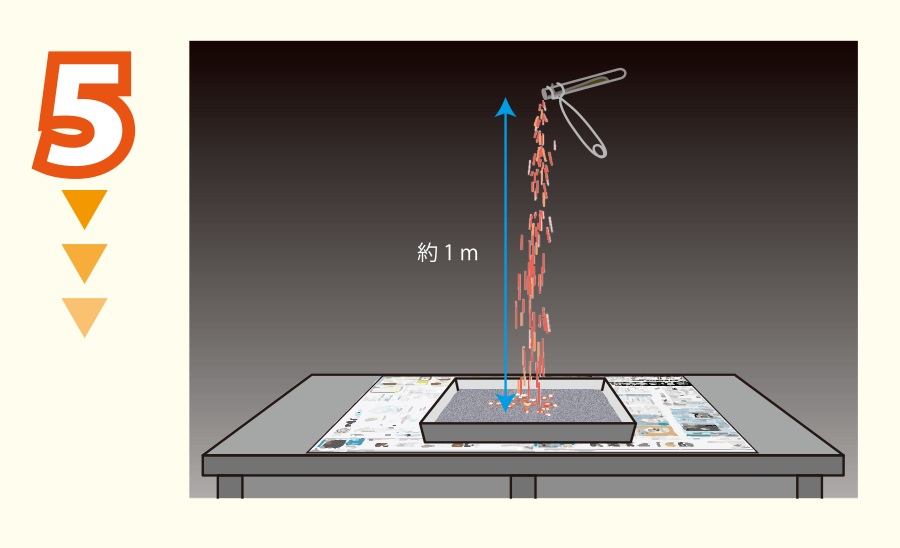
部屋の電気を消す。
試験管からコルク栓を外し,砂場の上約1 mの高さから,試験管内の黒色の粉末を少しずつパラパラと落とす。
実験の解説
シュウ酸鉄(Ⅱ)二水和物を加熱すると分解して,鉄や鉄の酸化物の黒色の粉末ができます。この粉末はとても細かく表面積が大きいため,反応しやすい性質があります。実験方法5で,試験管から黒色の粉末を少しずつパラパラと落とすとキラキラと光を発したのは,これらの粉末が空気中の酸素と反応し,自然発火したからです。
反応後は赤褐色の酸化鉄(Ⅲ)が生成します。実験後の砂場の上の生成物の色を観察してみましょう。
化学だいすきクラブニュースレター第57号(2024年7月1日発行)より編集/転載




